細胞周期停止と細胞死

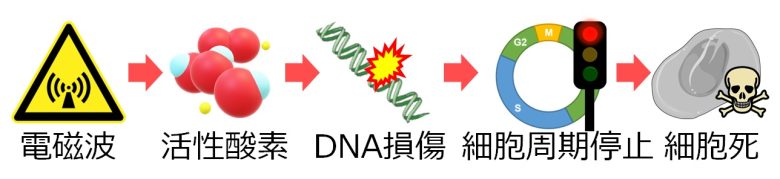
次に活性酸素がDNAを損傷し、さらに細胞周期を停止させることで、細胞死へと誘導する経路について説明します。
続いて電磁波によって細胞周期停止からの細胞死が、実際に起きたこと示す研究を紹介します。
目次All_Pages
細胞周期チェックポイント
前のぺージでは、活性酸素によってDNAが損傷、複製ストレスが発生し、突然変異が発生すると説明しました。
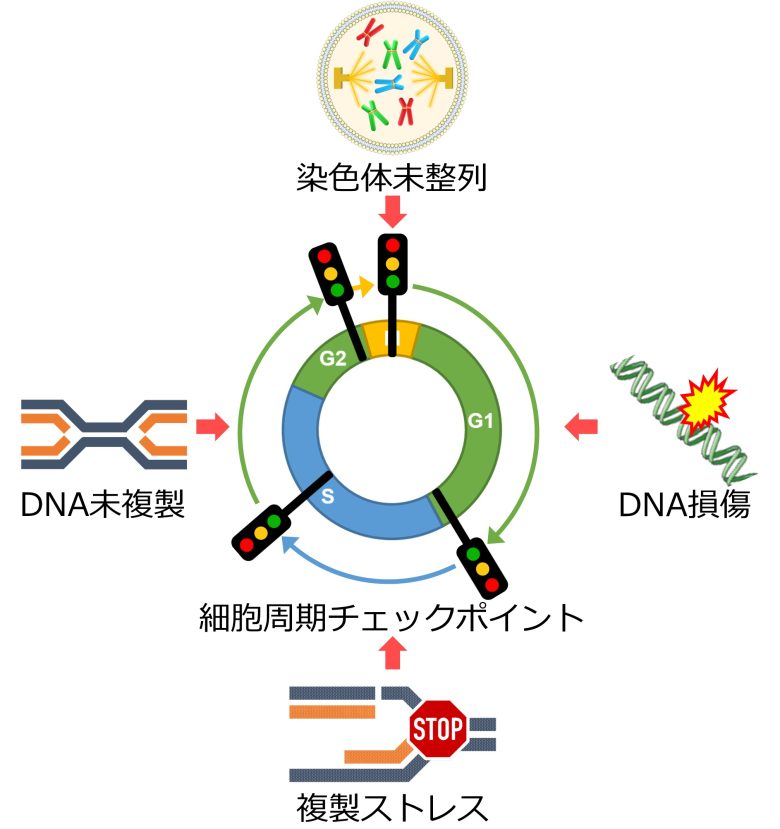
しかし実際にはこのような事態を防ぐため、DNA損傷や複製ストレスなどに応答して細胞周期を停止させてDNAの修復を試み、最悪でも細胞死させて遺伝子異常が伝搬するのを防ぐ機構が存在します。
この機構は細胞周期チェックポイントと呼ばれ、細胞周期の各所に設けられています。
サイクリン
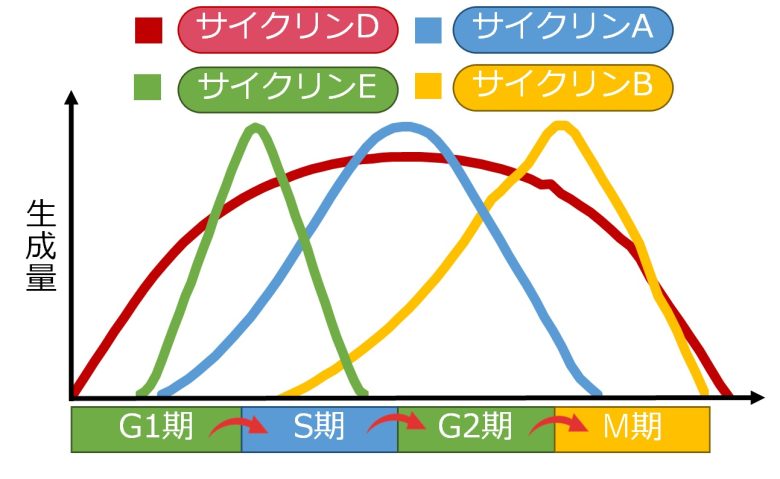
細胞周期の進行にはサイクリンと呼ばれるタンパク質の生成量が増加し、さらに活性化する必要があります。
G1期からS期の進行にはサイクリンDとE、S期の進行にはサイクリンA、G2期からM期への進行にはサイクリンBの生成量の増加が必要です。(Burhans and Heintz 2009)
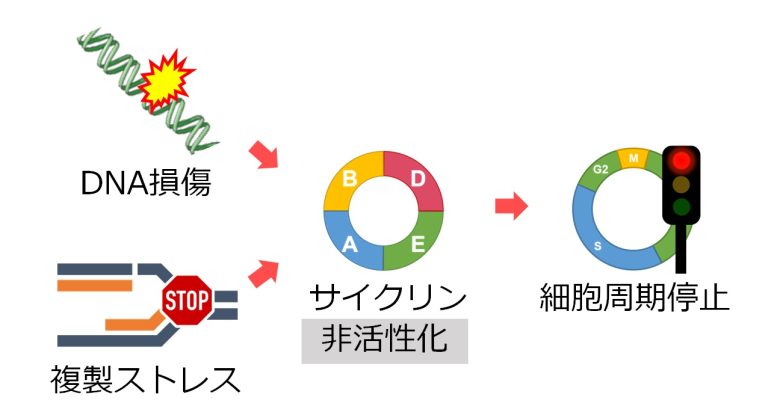
そしてDNA損傷や複製ストレスなどが起きた場合には、このサイクリンが非活性化することで、細胞周期の進行が停止します。
DNA損傷応答
細胞周期チェックポイントの中で、DNA損傷と複製ストレスに応答して細胞周期を止める機構はDNA損傷応答と呼ばれます。
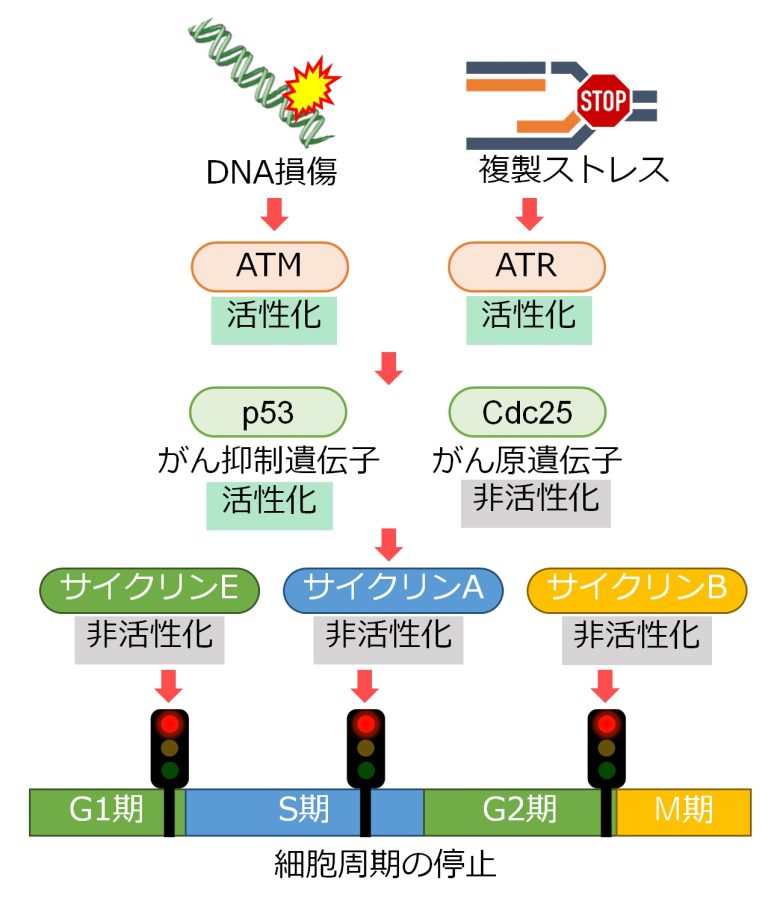
DNA損傷応答
(Rastogi et al. 2010から引用・改変)
- DNA損傷に応答してATM、複製ストレスに応答してATRというタンパク質がそれぞれ活性化する。
- すると、がん抑制遺伝子p53など、細胞周期を停止させるタンパク質が活性化する。
- また、がん原遺伝子Cdc25など、細胞周期を進行させるタンパク質が非活性化する。
- これをうけて、サイクリンE/A/Bが非活性化し、細胞周期が停止する。
細胞周期の停止の間には、DNAの修復が試みられます。(Burhans and Heintz 2009)
しかし、細胞周期停止が長期化すると、細胞死へと誘導されてしまいます。(Burhans and Heintz 2009)

活性酸素濃度と持続時間
活性酸素はその濃度と持続時間によって、細胞への影響が変わってきます。(Boonstra and Post 2004)
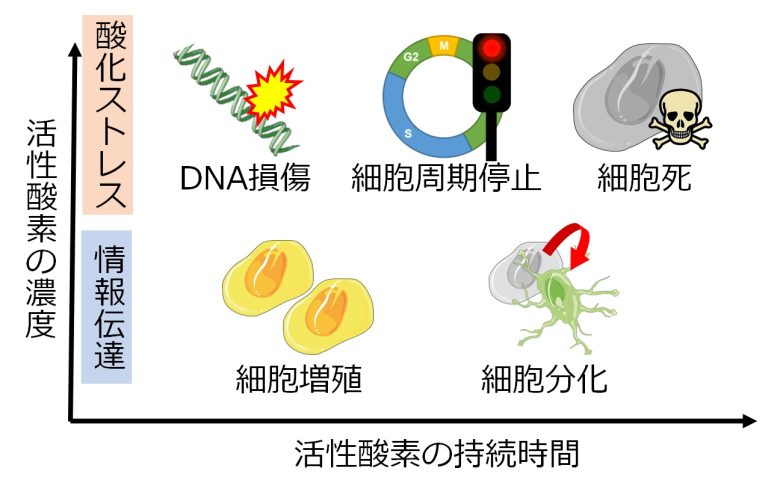
活性酸素の濃度と持続時間による細胞への影響
(Boonstra and Post 2004から引用・改変)
- 活性酸素が低濃度である場合、情報伝達という役割を果たし、短時間であれば細胞増殖、長時間であれば細胞分化などをもたらす。
- 活性酸素が高濃度である場合、酸化ストレスとなる。DNAは損傷し、細胞周期が停止する。それが長期化すると、細胞死へと誘導される。
細胞周期停止の長期化で細胞死
以上の話をまとめます。
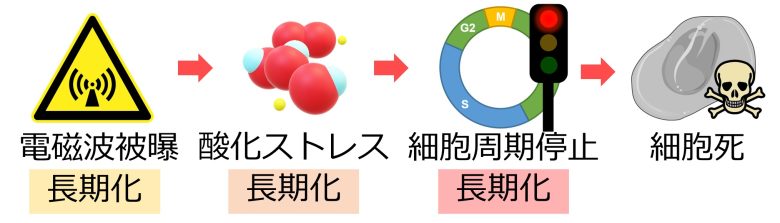
酸化ストレスの長期化は、細胞周期停止の長期化につながり、やがて細胞死に至ります。
また電磁波被曝が長期化すると、必然的に酸化ストレスが長期化します。
したがって長期間にわたって電磁波を照射すると細胞は死ぬ、という結論が導き出せます。
完全ではない細胞周期の機構
遺伝子異常が伝搬してしまうのを防ぐ細胞周期チェックポイントですが、その機構は完全ではありません。
まず細胞周期チェックポイントを構成する遺伝子自体が突然変異により機能しなくなった場合、チェックポイントは機能しなくなります。
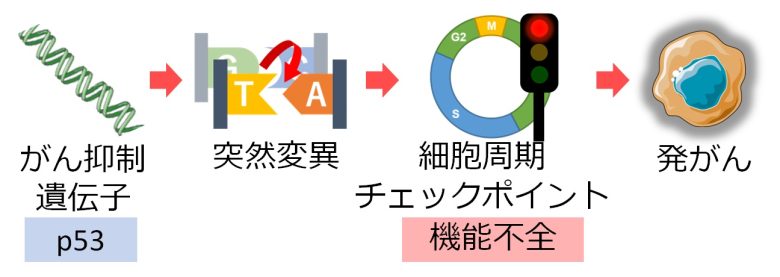
例えばがん抑制遺伝子p53が突然変異を起こすと発がんにつながると前のページで述べましたが、その理由の一つはp53が細胞周期チェックポイントを構成しているためです。
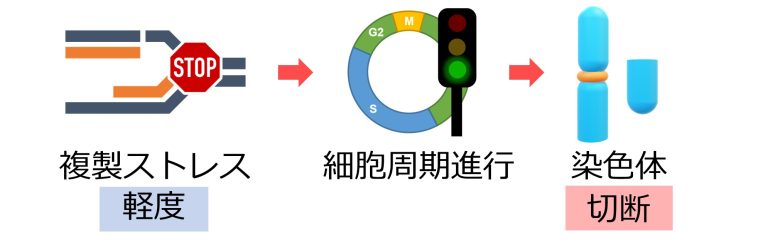
また、2013年のフランスの研究は、複製ストレスが軽度の場合、細胞周期は停止することなく進行し、細胞はDNAが未複製のまま細胞分裂に突入し、その結果、染色体が切断されることを発見しました。 (Koundrioukoff et al. 2013)
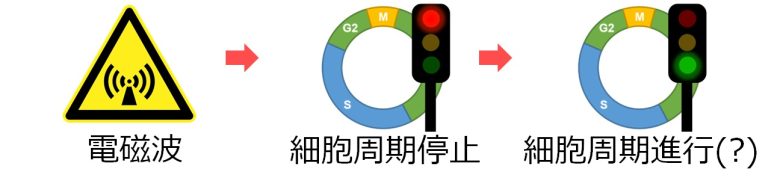
また、2002年のイギリスの研究は、ガンマ線照射によってDNAを損傷させて細胞周期を停止させた後、電磁波を継続的に照射すると逆に細胞周期を進行させることを発見しました。(Harris et al. 2002)
これは電磁波に細胞周期チェックポイントを弱める効果があることを示唆するものです。
この原因としては、電磁波が活性酸素の増加だけでなく、体内時計の乱れも引き起こすためと考えられます。
細胞内の体内時計は、時計遺伝子の刻む概日リズムです。これらの時計遺伝子は細胞周期チェックポイントの構成要素でもあるため (Sancar et al. 2010, Khapre et al. 2010)、時計遺伝子の刻む概日リズムの乱れは、細胞周期チェックポイントの機能不全につながるものと考えられます。
このように細胞周期チェックポイントを潜り抜けて突然変異を起こした細胞が生き残ると、がんや不妊や流産、遺伝子疾患など、より深刻な結果をもたらすものと考えられます。
電磁波で細胞周期停止と細胞死
ここで電磁波被曝により細胞周期が停止し、さらに細胞死が起きたことを示す研究を紹介します。
研究紹介
Xing et al. 2016
皮膚産生細胞であるマウス胚繊維芽細胞が、強さ121μW/cm2で1800 MHzの高周波電磁波を48時間被曝しました。
するとDNA損傷が増加し、がん抑制遺伝子p53の生成量が増加し、細胞死が増加しました。
DNA損傷に応答してp53が増加した結果、細胞周期が停止して最後には細胞死に至ったという経路が想定できます。
また抗酸化作用のあるN-アセチルシステイン (NAC) の投与は、上述の被害を抑制しました。
DNA損傷の増加
DNA損傷細胞の割合が、48時間の電磁波被曝で0%から60%まで増加しました。抗酸化作用のあるNACはそれを抑えました。
p53の生成量の増加
がん抑制遺伝子p53のタンパク質濃度が、48時間の電磁波被曝で2倍になりました。抗酸化作用のあるNACはそれを抑えました。これはDNAの損傷を抑えた結果と考えられます。
細胞死の増加
細胞死の指標が、48時間の電磁波被曝で4倍になりました。抗酸化作用のあるNACはそれを抑えました。
Huang et al. 2014
不死化ヒト角化細胞 (表皮細胞) が、強さ1.5 mTで60 Hzの低周波電磁波を144時間被曝しました。
すると細胞周期が停止し、細胞成長が阻害されました。
細胞周期の停止
電磁波被曝でG0/G1期の細胞が増加し、S期・G2/M期の細胞が減少しました。つまり細胞周期が停止しました。
細胞成長の阻害
細胞のコロニー数が、電磁波被曝で2割減少しました。つまり細胞成長が阻害されました。
Liu et al. 2003
マウスが強さ200 μTで50 Hzの低周波電磁波を2週間被曝しました。
すると肝細胞と脳細胞において、細胞周期が停止し、細胞死が増加しました。
細胞周期の停止
細胞死の増加
Kesari et al. 2011
局所SAR 0.9 W/kgの携帯電話を設置して待機中にし、青年に相当する生後10週のオスラットが近接してその電磁波を1日2時間、35日間被曝しました。
すると精液において、活性酸素が増加し、細胞周期が停止して細胞死が増加しました。
活性酸素の増加
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
細胞周期の停止
携帯電話の電磁波被曝でG0/G1期、S期、G2/M期の細胞が減少しました。つまり細胞周期が停止しました。
細胞死の増加
電磁波被曝で、細胞死の割合が2倍になりました。
Salem 2008
ブラウン管テレビを設置し、成体のオスラットが30cmの距離でその電磁波を1日6時間、2ヶ月間被曝しました。
すると表皮の細胞増殖が阻害されて細胞死が増加し、表皮・真皮の厚みが減少しました。
また、抗酸化作用のあるビタミンAの投与は、上述の被害を抑制しました。
細胞増殖の阻害
表皮の細胞増殖の指標が、ブラウン管テレビの電磁波被曝で4割減少しました。抗酸化作用のあるビタミンAはそれを抑えました。
細胞死の増加
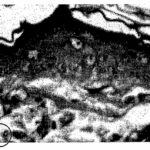
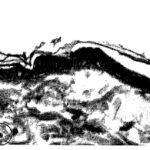
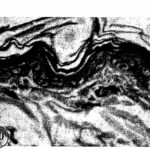
ブラウン管テレビの電磁波被曝で、表皮の細胞死が増加しました。抗酸化作用のあるビタミンAはそれを抑えました。
皮膚の厚みの減少
Pandey et al. 2016
青年に相当する生後8-10週のオスマウスが、携帯電話の電磁波に似せた高周波電磁波を、1日4時間か8時間、35日間被曝しました。
すると電磁波の1日の被曝時間が長くなるほど、精巣においてDNA切断が増加して細胞周期が停止し、精子の数が減少し、精子異常が増加しました。
また、被曝から時間が経つと上述の損傷はある程度回復しました。
DNAの切断はコメットアッセイで検出します。コメットアッセイにおいては、DNA切断が多くなるほど、Tail DNAは多くなり、Head DNAは少なくなり、Olive Tail Momentは大きくなります。
DNA切断の増加
細胞周期の停止
精子減少
精子異常の増加
Bin-Meferij and El-Kott 2015
局所SAR 0.96 W/kgの携帯電話の試験機を飼育ケージの中央に設置し、青年に相当する生後2ヶ月のオスラットがその電磁波を1日1時間、7週間被曝しました。
すると血液中の活性酸素が増加し、精巣の細胞増殖が阻害され、精子の数が減少しました。
また抗酸化作用のあるモリンガの投与は、上述の被害を抑制しました。
活性酸素の増加
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
細胞増殖の阻害 1

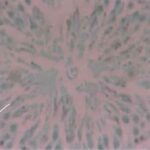
携帯電話の電磁波被曝で増殖中の細胞が減少しました。
細胞増殖の阻害 2
増殖中の細胞が、携帯電話の電磁波被曝で精巣で3割増加しました。抗酸化作用のあるモリンガはそれを幾分か抑えました。
精子減少
精子の数が、携帯電話の電磁波被曝で6割減少しました。抗酸化作用のあるモリンガはそれを抑えました。
実験の紹介は以上です。
実際に電磁波は細胞周期の停止させ、細胞死を引き起こすことを確認しました。

電磁波で細胞周期進行
ここで先ほど言及した、電磁波により逆に細胞周期が進行したことを示す研究を紹介します。
研究紹介
Harris et al. 2002
ヒト子宮頸がん細胞が、S期開始から4時間後に強さ 1・3・5 Gy のガンマ線を被曝しました。続けて強さ2 mTで50Hzの低周波電磁波を継続被曝しました。
するとS期開始から13時間後 (※) に、G2/M期の割合の細胞が減少し、次のG1期の細胞の割合が増加しました。つまりガンマ線によるDNA損傷で停止した細胞周期を、電磁波は逆に進行させました。
5 Gyのガンマ線では15時間後
一方、電磁波のみの被曝では、幾分か細胞周期が停止しました。
この結果は、電磁波に細胞周期チェックポイントを弱める効果があることを示唆します。

