前回の記事では、電磁波が健康に悪影響を及ぼすことを示した多数の研究を紹介しました。
この記事では続いて、その仕組みについて説明します。
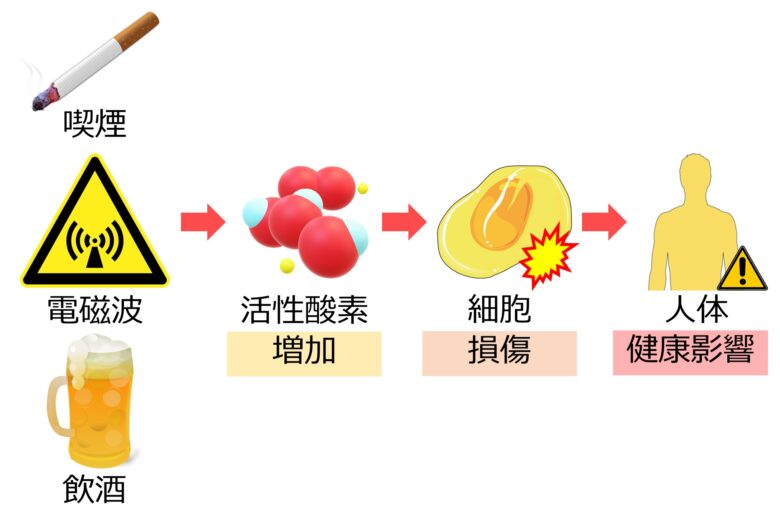
電磁波は主として活性酸素を増加させることで、健康に悪影響を与えることが分かってきています。
まずはじめに、電磁波が実際に活性酸素を発生させることを示した、多数の研究を紹介します。
続いて活性酸素が細胞レベルでどのように損傷を引き起こすのか、またそれがどのように数々の疾患へとつながるのか、その仕組みを説明します。
その説明の中で、DNA損傷、突然変異、染色体異常、細胞周期停止、ミトコンドリア損傷、免疫反応、細胞死といった、電磁波が活性酸素による細胞損傷を引き起こすことを示した、様々な研究を都度紹介します。
電磁波が健康に影響を与えることを示した多数の研究は、以下の記事からご覧いただけます。

今のご時勢、電磁波が体に悪いと言うと、ちょっと非常識な人だと思われるかもしれません。 しかし、これは実際に数多くの科学論文が指し示していることなのです。 私も実際に自分の目で確かめてみるまでは、半信半… 記事全文を読む

石塚 拓磨
北海道函館市在住。大学では情報工学を専攻し、エンジニアとして10年以上の経験があります。
このサイトを通じて少しでも多くの人が電磁波の危険性について気づいていただければ幸いです。
概要

まず、電磁波が活性酸素を増加させたことを示す研究を紹介します。
続いて活性酸素がどのように健康へ影響を与えるのか、その概要を説明します。
活性酸素とは何か?
多くの生物にとって酸素は必要不可欠な存在ですが、同時に有害な存在でもあります。
なぜなら呼吸の過程で、酸素の一部が不安定で反応性の高い、活性酸素へと変化してしまうためです。
活性酸素は免疫機能や細胞の情報伝達に必須の存在ですが、過剰な量になると細胞を損傷し、健康を害する要因となります。
そのため生体においては活性酸素を無害化する抗酸化物質が存在し、活性酸素による損傷を防いでいます。
しかし、抗酸化物質で防げない量まで活性酸素が増加してしまうと、細胞が損傷をうけ、人の健康に影響を与えます。
活性酸素を増加させる要因としては、喫煙や飲酒などがよく知られていますが、実は電磁波も、活性酸素を増加させる要因のうちの一つです。

電磁波による活性酸素の増加
電磁波によって活性酸素が増加したことを示す、非常に多数の研究が存在します。
例えば、2022年に更新されたバイオイニシャティブ2012の報告では、586件の研究のうち、533件の研究が電磁波による酸化損傷を認めています。(Bioinitiative 2022)
また、高周波電磁波の生物学的影響に関する総説によると、100件の研究のうち93件が、低強度の高周波電磁波が酸化作用を生体に引き起こすことを実証しています。 (Yakymenko et al. 2015)
またいくつかの研究では、抗酸化物質を摂取することで、電磁波による損傷を抑えられることを示してします。
これは電磁波による損傷が、活性酸素の増加に由来することを示すものです。
研究紹介
このサイトで紹介している研究のうち、活性酸素の増加を示す24の研究を紹介します。
中国の陝西省の遺伝クリニックに通う男性について、スマホ・携帯基地局・Wi-Fiからの1日あたりの電磁波の被曝時間が増加するほど、精液中の活性酸素が増加し、精子の数が減少しました。
活性酸素の増加
活性酸素濃度が、スマホ・携帯基地局・Wi-Fiの電磁波の1日2時間超の被曝で7割増加しました。
総抗酸化能が、スマホ・携帯基地局・Wi-Fiの電磁波の1日2時間超の被曝で7割減少しました。
グルタチオンペルオキシダーゼの抗酸化活性が、スマホ・携帯基地局・Wi-Fiの電磁波の1日2時間超の被曝で5割減少しました。
スーパーオキシドディスムターゼの抗酸化活性が、スマホ・携帯基地局・Wi-Fiの電磁波の1日2時間超の被曝で6割減少しました。
ROSTOCGSH-PxSOD
総抗酸化能、抗酸化活性の減少は活性酸素の増加を意味します。
精子減少
精子の数が、スマホ・携帯基地局・Wi-Fiの電磁波の1日2時間超の被曝で7割減少しました。
局所SAR 0.96 W/kgの携帯電話の試験機を飼育ケージの中央に設置し、青年に相当する生後2ヶ月のオスラットがその電磁波を1日1時間、7週間被曝しました。
すると血液中の活性酸素が増加し、精子の数が減少しました。
また抗酸化作用のあるモリンガの投与は、上述の被害を抑制しました。
活性酸素の増加
脂質過酸化の指標であるマロンジアルデビドが、携帯電話の電磁波被曝で2倍になりました。抗酸化作用のあるモリンガはそれを抑えました。
カタラーゼの抗酸化活性が、携帯電話の電磁波被曝で5割減少しました。抗酸化作用のあるモリンガはそれを抑えました。
スーパーオキシドディスムターゼの抗酸化活性が、携帯電話の電磁波被曝で3割減少しました。抗酸化作用のあるモリンガはそれを抑えました。
MDACATSOD
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
精子減少
精子の数が、携帯電話の電磁波被曝で6割減少しました。抗酸化作用のあるモリンガはそれを抑えました。
局所SAR 1.34 W/kgの携帯電話を設置して1日2時間会話中にし、青年に相当する生後10週のオスラットが近接してその電磁波を60日間被曝しました。
すると精子の活性酸素が増加し、精子の数が減少しました。
活性酸素の増加
精子の脂質過酸化の指標であるTBARSが、携帯電話の電磁波被曝で6割増加しました。
脂質過酸化の増加は活性酸素の増加を意味します。
精子減少
精子の数が、携帯電話の電磁波被曝で2割減少しました。
メスラットをオスラットと交尾させ、受精を確認しました。
続けてメスラットが、携帯電話の電磁波に似せた高周波電磁波を、全身平均SAR 0.048 W/kgで1日1時間か2時間被曝しました。
被曝期間は妊娠初期の1週間、あるいは妊娠初期・中期の2週間、あるいは妊娠全期の3週間のいずれかでした。
すると電磁波の被曝時間と期間が長くなるほど、胎児血液中の活性酸素が増加し、不妊・流産が増加しました。
活性酸素の増加
胎児血液中の脂質過酸化の指標であるマロンジアルデビドが、妊娠中の電磁波の被曝が長くなるほど増加しました。
胎児血液中のグルタチオンペルオキシダーゼの抗酸化活性が、妊娠中の電磁波の被曝が長くなるほど減少しました。
MDAGSH-Px
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
不妊・流産の増加
妊娠初期の電磁波被曝で生まれた子どもの数に変化はありません。
生まれた子どもの数が、妊娠初期から中期の1日2時間の電磁波被曝で4割減少しました。不妊・流産が増加したといえます。
生まれた子どもの数が、妊娠全期の1日2時間の電磁波被曝で4割減少しました。不妊・流産が増加したといえます。
1週間2週間3週間
メスラットが50 Hz、8 mTの低周波電磁波を40日間被曝しました。
すると卵胞の顆粒膜細胞の細胞死が増加しました。
また抗酸化作用のあるスイートバジルの投与は、上述の被害をある程度抑制しました。
細胞死の増加
顆粒膜細胞の細胞死の割合が、電磁波被曝で4倍になりました。抗酸化作用のあるスイートバジルはそれをある程度抑えました。
妊娠中のメスラットが2450 MHzの高周波電磁波を全身平均SAR 0.143 W/kgで1日1時間、妊娠全期の3週間被曝し、さらに生まれた娘ラットが生後3週から思春期の始まり (子ども期に相当) まで被曝しました。
すると脳と卵巣において活性酸素が増加し、ホルモンバランスが乱れ、思春期の始まりが遅れました。
活性酸素の増加
卵巣の酸化ストレス指数が、子ども期の電磁波被曝で1.6倍、胎児期と子ども期の被曝で1.9倍になりました。
脳の酸化ストレス指数が、子ども期の電磁波被曝で2.2倍、胎児期と子ども期の被曝で1.9倍になりました。
卵巣脳
酸化ストレスの増加は活性酸素の増加を意味します。
ホルモンバランスの乱れ
黄体形成ホルモンの血中濃度が、子ども期の電磁波被曝で9割増、胎児期と子ども期の被曝で6割増加しました。
インスリン様成長因子1の血中濃度が、子ども期の電磁波被曝で4割減、胎児期と子ども期の被曝で2割減少しました。
卵巣刺激ホルモンの血中濃度が、子ども期の電磁波被曝で4割増、胎児期と子ども期の被曝で変化無しです。
LHIGF-1FSH
思春期の始まりの遅れ
発情期の始まりが、子ども期の電磁波被曝で2割、胎児期と子ども期の被曝で3割遅れました。
オスラットが900MHz、1800MHz、2450MHzの高周波電磁波をそれぞれ全身平均SAR 0.00059 W/kg、0.00058 W/kg、0.00066 W/kgで1日2時間、60日間被曝しました。
するとラットの海馬において、電磁波の周波数が高くなるほど、活性酸素が増加し、炎症反応が増加し、DNA切断が増加しました。
活性酸素の増加
海馬において脂質過酸化の指標であるマロンジアルデビドが、電磁波の周波数が高くなるほど増加しました。
海馬においてグルタチオンの抗酸化活性が、電磁波の周波数が高くなるほど減少しました。
海馬においてスーパーオキシドディスムターゼの抗酸化活性が、電磁波の周波数が高くなるほど減少しました。
海馬においてカタラーゼの抗酸化活性が、電磁波の周波数が高くなるほど逆に増加しました。
MDAGSHSODCAT
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
炎症反応の増加は、炎症反応を促進する働きをもつ、炎症性サイトカインの増加で示されました。
炎症反応の発生
海馬において炎症性サイトカインであるTNF-αが、2450 MHzの高周波電磁波の被曝で7割増加しました。
海馬において炎症性サイトカインであるIFN-γが、2450 MHzの高周波電磁波の被曝で2.6倍になりました。
海馬において炎症性サイトカインであるIL-6が、2450 MHzの高周波電磁波の被曝で、7割増加しました。
海馬において炎症性サイトカインであるIL-2が、2450 MHzの高周波電磁波の被曝で2.7倍になりました。
TNF-αIFN-γIL-6IL-2
DNAの切断はコメットアッセイで検出します。コメットアッセイにおいては、DNA切断が多くなるほど、Tail DNAは多くなり、Tail Lengthは長くなり、Olive Tail Momentは大きくなります。
DNA切断の増加
海馬においてDNA切断の指標であるTail DNAが、2450 MHzの高周波電磁波の被曝で2.7倍になりました。
海馬においてDNA切断の指標であるTail Lengthが、2450 MHzの高周波電磁波の被曝で4.0倍になりました。
海馬においてDNA切断の指標であるOlive Tail Momentが、2450 MHzの高周波電磁波の被曝で3.4倍になりました。
Tail DNATail LengthOlive Tail Moment
成人に相当する生後10-12週のオスマウスが、強さ200μTで50 Hzの低周波電磁波を1日8時間、30日間被曝しました。
続いてマウスにモーリスの水迷路テストを受けさせました。
すると脳内における活性酸素が増加し、マウスは記憶力の低下を示しました。
また抗酸化作用のあるカテキン・エピカテキンの投与は、上記の被害を抑制しました。
活性酸素の増加
脂質過酸化の指標であるマロンジアルデビドが、電磁波被曝で2倍になりました。抗酸化作用のあるカテキン・エピカテキンの投与はそれを抑えました。
スーパーオキシドディスムターゼの抗酸化活性が、電磁波被曝で7割減少しました。抗酸化作用のあるカテキン・エピカテキンの投与はそれを抑えました。
カタラーゼの抗酸化活性が、電磁波被曝で5割減少しました。抗酸化作用のあるカテキン・エピカテキンの投与はそれを抑えました。
脂質酸化抗酸化物質 1抗酸化物質 2
モーリスの水迷路テスト
まずモーリスの水迷路テストの訓練を1日4回、6日連続で実施します。
 (ULTRABEMから引用)
(ULTRABEMから引用)そして6日目の最後の訓練から3時間後に、逃避台を除去して試験を実施します。
逃避台があった場所への到達時間と、滞在時間で記憶力を評価します。

記憶力の低下
逃避台があった場所への到達時間が、電磁波被曝で2割増加しました。つまりマウスは逃避台の場所を忘れてしまっており、記憶力が低下したと言えます。抗酸化作用のあるカテキン・エピカテキンの投与はそれを抑えました。
逃避台があった場所での滞在時間が、電磁波被曝で3割減少しました。つまりマウスは逃避台の場所を忘れてしまっており、記憶力が低下したと言えます。抗酸化作用のあるカテキン・エピカテキンの投与はそれを抑えました。
到達時間滞在時間
成体のオスラットが強さ3mTで50Hzの低周波電磁波を1日4時間、2ヶ月間被曝しました。
すると心臓において活性酸素が増加し、心筋の細胞死が増加しました。
活性酸素の増加
脂質過酸化の指標であるマロンジアルデビドが、電磁波被曝で4倍になりました。
スーパーオキシトディスムターゼの抗酸化活性が、電磁波被曝で4割減少しました。
グルタチオンペルオキシダーゼの抗酸化活性が、電磁波被曝で4割減少しました。
MDASODGSH-Px
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
細胞死の増加
心筋の細胞死のスコアが、電磁波被曝で2倍になりました。
心筋の細胞死の割合が、電磁波被曝で2倍になりました。
細胞死 1細胞死 2
妊娠中のラットが強さ1 mW/cm2で900MHzの高周波電磁波を妊娠全期の3週間被曝しました。
すると生まれた息子ラットの肺の成長が阻害されました。
また抗酸化作用のあるメラトニンの投与は、上述の被害を抑制しました。
肺の成長阻害
息子ラットの細気管支の体積が、妊娠中の電磁波被曝で6割減少しました。抗酸化作用のあるメラトニンはそれを抑えました。
息子ラットの肺胞の体積が、妊娠中の電磁波被曝で3割減減です。抗酸化作用のあるメラトニンはそれを抑えました。
息子ラットの肺血管の体積が、妊娠中の電磁波被曝で2割減少しました。抗酸化作用のあるメラトニンはそれを抑えました。
細気管支肺胞肺血管
大人のオスラットが950 MHzの高周波電磁波を1日1時間、50日間被曝しました。
すると肺と心臓と血液中において活性酸素が増加し、臓器損傷の指標であるLDH (乳酸脱水素酵素) が増加しました。
また抗酸化作用のある紅茶キノコの投与は、上述の被害を抑制しました。
肺の活性酸素の増加
肺の脂質過酸化の指標であるマロンジアルデビドが、電磁波被曝で7割増加しました。抗酸化作用のある紅茶キノコはそれを抑えました。
肺のグルタチオンペルオキシダーゼの抗酸化活性が、電磁波被曝で3割減少しました。抗酸化作用のある紅茶キノコはそれを抑えました。
肺のスーパーオキシドディスムターゼの抗酸化活性が、電磁波被曝で逆に3割増加しました。
MDAGSH-PxSOD
心臓の活性酸素の増加
心臓の脂質過酸化の指標であるマロンジアルデビドが、電磁波被曝で5割増加しました。抗酸化作用のある紅茶キノコはそれを抑えました。
心臓のグルタチオンペルオキシダーゼの抗酸化活性が、電磁波被曝で6割減少しました。抗酸化作用のある紅茶キノコはそれを抑えました。
心臓のスーパーオキシドディスムターゼの抗酸化活性が、電磁波被曝で逆に2割増加しました。
MDAGSH-PxSOD
血液中の活性酸素の増加
血液中の総抗酸化能が、電磁波被曝で6割減少しました。抗酸化作用のある紅茶キノコはそれを抑えました。
脂質過酸化の増加と抗酸化活性と総抗酸化能の減少は、活性酸素の増加を意味します。
臓器損傷の増加
臓器損傷の指標であるLDH (乳酸脱水素酵素) 活性が、電磁波被曝で2割増加しました。抗酸化作用のある紅茶キノコはそれを抑えました。
大人のオスラットが強さ5μTで50Hzの低周波電磁波を1日5分、隔日で6か月被曝しました。
すると肺と肝臓において活性酸素が増加しました。
また抗酸化作用のある亜鉛の投与は、上述の被害を抑制しました。
活性酸素の増加
脂質過酸化の指標であるマロンジアルデビドが、電磁波被曝で4倍になりました。抗酸化作用のある亜鉛はそれを抑えました。
脂質過酸化の指標であるマロンジアルデビドが、電磁波被曝で6倍になりました。抗酸化作用のある亜鉛はそれを抑えました。
肺肝臓
脂質過酸化の増加は活性酸素の増加を意味します。
Wi-Fi-ルータを設置して1日4時間データ通信中にし、青年に相当する生後12週のオスラットが30cmの距離でその電磁波を45日間被曝しました。
すると膵臓において活性酸素が増加し、ランゲルハンス島のインスリン分泌能が低下しました。
活性酸素の増加
脂質過酸化の指標であるマロンジアルデビドが、Wi-Fiの電磁波被曝で3倍になりました。
グルタチオンの抗酸化活性が、Wi-Fiの電磁波被曝で3割減少しました。
スーパーオキシドディスムターゼの抗酸化活性が、Wi-Fiの電磁波被曝で3割減少しました。
グルタチオンペルオキシダーゼの抗酸化活性が、Wi-Fiの電磁波被曝で4割減少しました。
MDAGSHSODGSH-Px
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
続いてランゲルハンス島のインスリン分泌能の結果です。
これはマウスから摘出したランゲルハンス島に、低濃度あるいは高濃度のブドウ糖を曝した時の、インスリン分泌量を比較したものです。
インスリン分泌能の低下
ランゲルハンス島のインスリン分泌能が、Wi-Fiの電磁波被曝で低下しました。インスリン分泌量が、低濃度のブドウ糖への曝露で2割、高濃度で5割減少しました。
妊娠中のラットが強さ54 μW/cm2で900MHzの高周波電磁波を1日1時間、妊娠後期の1週間被曝しました。
すると生まれた息子ラットの肝臓で活性酸素が増加しました。
活性酸素の増加
息子ラットの脂質過酸化の指標であるマロンジアルデビドが、妊娠中の電磁波被曝で4割増加しました。
息子ラットのグルタチオンの抗酸化活性が、妊娠中の電磁波被曝で4割減少しました。
息子ラットのスーパーオキシドディスムターゼの抗酸化活性が、妊娠中の電磁波被曝で逆に2割増加しました。
MDAGSHSOD
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
青年に相当する生後16-20週のラットが、2100MHzの高周波電磁波を全身平均SAR 0.024 W/kgで1日6-12時間、30日間被曝しました。
すると腎臓で活性酸素が増加し、細胞死が増加し、尿細管が壊死しました。
尿細管は原尿から水分や必要な物質を再吸収する組織です。
活性酸素の増加
脂質過酸化の指標であるマロンジアルデビドが、1日12時間の電磁波被曝で2割増加しました。
グルタチオンの抗酸化活性が、1日12時間の電磁波被曝で1割減少しました。
MDAGSH
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
細胞死の増加
腎臓の細胞死のスコアが、電磁波の被曝期間が長くなるほど増加しました。
尿細管の壊死
尿細管壊死のスコアが、電磁波の被曝期間が長くなるほど、増加しました。
青年に相当する生後8週のラットが900MHzの高周波電磁波を1日1時間、10日間被曝しました。
すると腎臓において活性酸素が増加し、尿細管が損傷しました。
抗酸化作用のあるメラトニンの投与は上述の被害を抑制しました。
活性酸素の増加
脂質過酸化の指標であるマロンジアルデビドが、電磁波被曝で9割増加しました。抗酸化作用のあるメラトニンはそれを抑えました。
カタラーゼの抗酸化活性が、電磁波被曝で2割減少しました。抗酸化作用のあるメラトニンはそれを抑えました。
スーパーオキシドディスムターゼの抗酸化活性が、電磁波被曝で3割減少しました。抗酸化作用のあるメラトニンはそれを抑えました。
グルタチオンペルオキシダーゼの抗酸化活性が、電磁波被曝で2割減少しました。抗酸化作用のあるメラトニンはそれを抑えました。
MDACATSODGSH-Px
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
尿細管の損傷
尿細管損傷の指標である尿中NAGが、電磁波被曝で5倍になりました。抗酸化作用のあるメラトニンはそれを抑えました。
局所SAR 1.2 W/kgの携帯電話を飼育ケージの上に設置し、1日40分間着信中にし、子どもに相当する生後6週のメスラットがその電磁波を4週間被曝しました。
すると角膜において活性酸素が増加しました。水晶体においては活性酸素の増加と減少の双方が示唆されました。
抗酸化作用のあるビタミンCの投与は、角膜における被害を抑制しました。
角膜の活性酸素の増加
角膜の脂質過酸化の指標であるマロンジアルデビドが、携帯電話の電磁波被曝で10倍になりました。抗酸化作用のあるビタミンCの投与はそれを抑えました。
角膜のスーパーオキシドディスムターゼの抗酸化活性が、携帯電話の電磁波被曝で5割増加しました。抗酸化作用のあるビタミンCの投与はそれを抑えました。
角膜のグルタチオンペルオキシダーゼの抗酸化活性が、携帯電話の電磁波被曝で1割減少しました。抗酸化作用のあるビタミンCの投与はそれを抑えました。
角膜のカタラーゼの抗酸化活性が、携帯電話の電磁波被曝で逆に3倍になりました。
MDASODGSH-PxCAT
水晶体の活性酸素の増加
水晶体の脂質過酸化の指標であるマロンジアルデビドが、携帯電話の電磁波被曝で2倍になりました。抗酸化作用のあるビタミンCはそれを抑えました。
水晶体のスーパーオキシドディスムターゼの抗酸化活性が、携帯電話の電磁波被曝で逆に2割増加しました。
携帯電話の電磁波被曝で水晶体のグルタチオンペルオキシダーゼの抗酸化活性に変化はありませんでした。
水晶体のカタラーゼの抗酸化活性が、携帯電話の電磁波被曝で逆に3割増加しました。
MDASODGSH-PxCAT
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
青年に相当する生後5-6ヵ月のラットが、パルス変調した強さ3.6 μW/cm2で2.45 GHzの高周波電磁波を1日1時間、30日間被曝しました。
すると脳内と血液中において活性酸素が増加し、DNA酸化が増加しました。
また抗酸化作用のあるニンニクの投与は、上述の被害を抑制しました。
活性酸素の増加
脂質過酸化の指標であるTBARSが、電磁波被曝で2割増加しました。抗酸化作用のあるニンニクはそれをある程度抑えました。
DNA酸化の増加
DNA酸化の指標である8OHdGが、電磁波被曝で3倍になりました。抗酸化作用のあるニンニクはそれを抑えました。
DNA酸化の指標である8OHdGが、電磁波被曝で3倍になりました。抗酸化作用のあるニンニクはそれをある程度抑えました。
脳内血液中
中国吉林大学第一病院で募った研究参加者について、高圧線の電磁波の職業被曝を受けていると、尿中において活性酸素が増加し、DNA酸化が増加しました。
また抗酸化作用のある緑茶ポリフェノールサプリの服用は、上述の被害を抑制しました。
活性酸素の増加
脂質過酸化の指標であるイソプラスタンが、高圧線の電磁波被曝で5割増加しました。抗酸化作用のある緑茶ポリフェノールサプリはそれを抑えました。
DNA酸化の増加
DNA酸化の指標である8OHdGが、高圧線の電磁波被曝で4割増加しました。抗酸化作用のある緑茶ポリフェノールサプリはそれを抑えました。
青年に相当する生後8-12週のラットが、強さ500μTで60Hzの低周波電磁波を2時間被曝しました。
すると脳内のDNAの一重鎖切断と二重鎖切断が増加しました。
また、抗酸化作用のあるビタミンE、鉄キレート剤 (※) の投与は、上述の被害を抑制しました。
鉄イオンを封鎖することで、過酸化水素がヒドロキシルラジカルへと変化する反応を抑えます。
DNAの切断は細胞を電気泳動にかけて検出します。電気泳動においては、DNA切断が多くなるほど、DNA移動距離が増加します。
DNA切断の増加
DNA一重鎖切断の指標であるDNA移動距離が、低周波電磁波の被曝で4割増加しました。抗酸化作用のあるビタミンEと鉄キレート剤の投与はそれを抑えました。
DNA二重鎖切断の指標であるDNA移動距離が、低周波電磁波の被曝で1割増加しました。抗酸化作用のあるビタミンEと鉄キレート剤の投与はそれを抑えました。
一重鎖切断二重鎖切断
インドのミゾラム州アイザウルの研究参加者において、自宅から携帯基地局までの距離が短くなるほど、血液中の活性酸素が増加し、血中リンパ球で微小核が増加しました。
高周波電磁波の強さは、携帯基地局の300m圏外で平均 0.0035 μW/cm2、80m圏内で平均 0.5 μW/cm2でした。
活性酸素の増加
脂質過酸化の指標であるTBARSが、携帯基地局の20m圏内で、7割増加しました。
グルタチオンの抗酸化活性が、携帯基地局の20m圏内で、2割減少しました。
カタラーゼの抗酸化活性が、携帯基地局の20m圏内で、5割減少しました。
スーパーオキシドディスムターゼの抗酸化活性が、携帯基地局の20m圏内で、4割減少しました。
TBARSGSHCATSOD
脂質過酸化の増加、抗酸化活性の減少は活性酸素の増加を意味します。
微小核の増加
微小核の頻度が、携帯基地局の20m圏内で、7割増加しました。
局所SAR 0.9 W/kgの携帯電話を設置して待機中にし、青年に相当する生後10週のオスラットが近接してその電磁波を1日2時間、35日間被曝しました。
すると精液において、活性酸素が増加し、細胞周期が停止して細胞死が増加しました。
活性酸素の増加
活性酸素濃度が、携帯電話の電磁波被曝で4割増加しました。
脂質過酸化の指標であるTBARSが、携帯電話の電磁波被曝で2倍になりました。
グルタチオンペルオキシダーゼの抗酸化活性が、携帯電話の電磁波被曝で4割減少しました。
スーパーオキシドディスムターゼの抗酸化活性が、携帯電話の電磁波被曝で2割減少しました。
カタラーゼの抗酸化活性が、携帯電話の電磁波被曝で逆に4割増加しました。
ROSTBARSGSH-PxSODCAT
脂質過酸化の増加と抗酸化活性の減少は活性酸素の増加を意味します。
細胞周期の停止
携帯電話の電磁波被曝でG0/G1期、S期、G2/M期の細胞が減少しました。つまり細胞周期が停止しました。
細胞死の増加
ブラウン管テレビを設置し、成体のオスラットが30cmの距離でその電磁波を1日6時間、2ヶ月間被曝しました。
すると細胞増殖が阻害され、表皮・真皮の厚みが減少しました。
また、抗酸化作用のあるビタミンAの投与は、上述の被害を抑制しました。
細胞増殖の阻害
表皮の細胞増殖の指標が、ブラウン管テレビの電磁波被曝で4割減少しました。抗酸化作用のあるビタミンAはそれを抑えました。
皮膚の厚みの減少
表皮の厚さが、ブラウン管テレビの電磁波被曝で5割減少しました。抗酸化作用のあるビタミンAはそれを抑えました。
真皮の厚さが、ブラウン管テレビの電磁波被曝で3割減少しました。抗酸化作用のあるビタミンAはそれを抑えました。
表皮の厚み真皮の厚み
皮膚産生細胞であるマウス胚繊維芽細胞が、強さ121μW/cm2で1800 MHzの高周波電磁波を48時間被曝しました。
するとDNA損傷が増加し、細胞死が増加しました。
また抗酸化作用のあるN-アセチルシステイン (NAC) の投与は、上述の被害を抑制しました。
DNA損傷の増加
DNA損傷細胞の割合が、48時間の電磁波被曝で0%から60%まで増加しました。抗酸化作用のあるNACはそれを抑えました。
細胞死の増加
細胞死の指標が、48時間の電磁波被曝で4倍になりました。抗酸化作用のあるNACはそれを抑えました。
実験の紹介は以上です。
実際に電磁波は活性酸素を増加させて健康に様々な影響を与えていることを確認しました。

もっとみる (5件)
酸化ストレスによる数々の疾患
活性酸素が細胞に損傷を与えるレベルまで増加した状態のことを酸化ストレスといいます。
そしてこの酸化ストレスは、数々の疾患に関与しています。
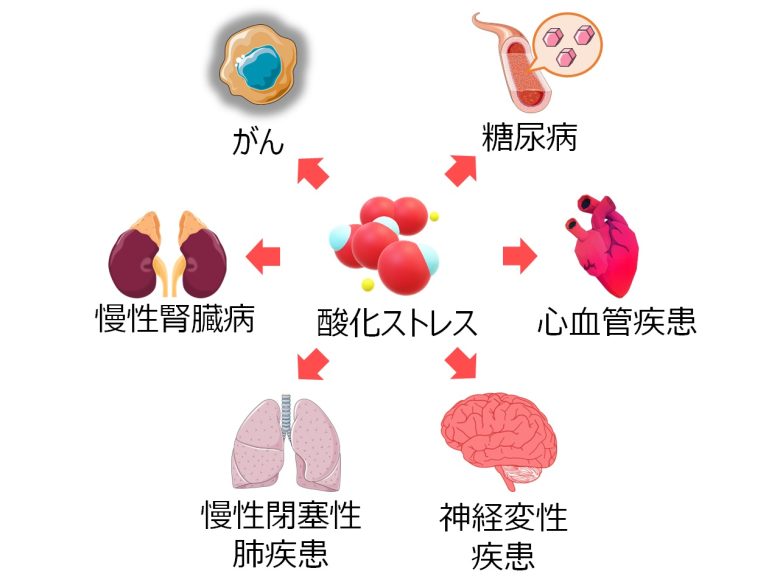
老化に関わる様々な病気
酸化ストレスは、糖尿病、心血管疾患、慢性閉塞性肺疾患、慢性腎臓病、神経変性疾患、がんなど、老化に伴うさまざまな疾患に関与しています。 (Liguori et al. 2018)
従って、酸化ストレスが老化自体をもたらしているという可能性が示唆されます。(Liguori et al. 2018)

喫煙と慢性閉塞性肺疾患
喫煙は肺に酸化ストレスと免疫反応を引き起こし、これらの相互作用によって慢性閉塞性肺疾患をもたらします。(Zuo et al. 2014)

アルコールと肝疾患
アルコールは肝臓に酸化ストレスを引き起こすことで、様々な肝疾患をもたらします。(Albano 2006)

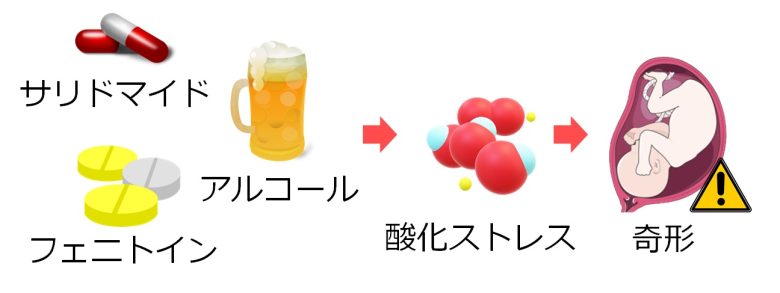
サリドマイドと奇形
サリドマイドや抗てんかん薬であるフェニトイン、アルコールなどの催奇形因子は、酸化ストレスを引き起こすことで、胎児に奇形を引き起こします。 (Dennery 2007)

流産・胎芽病・胎児発育不全・早産・低出生体重児
酸化ストレスは、流産、胎芽病 (胚・胎児の発達異常)、胎児発育不全、早産、低出生体重など、妊娠に関連するさまざまな疾患の促進因子として浮上しています。(Al-Gubory et al. 2010)
例えば、流産された女性、胎児発育不全の女性において、胎盤における活性酸素の増加がみられました。(Hempstock et al. 2003, Biri et al. 2007)
マウスを使った実験では、遺伝子操作によって活性酸素を過剰に発生させると、低出生体重児が生まれ、新生児の発育が遅れました。(Ishii et al. 2011)

男性不妊
精巣は特に酸化ストレスの影響を受けやすく、男性不妊の重要な要因です。(Asadi et al. 2017)
例えば、不妊男性のDNAの酸化損傷は、妊孕男性の100倍にも上るという研究報告があります。(Asadi et al. 2017)
マウスを使った実験では、農薬や抗がん剤などに起因する酸化ストレスにより、精巣におけるDNA損傷や細胞死が増加し、精子数の減少や精子劣化をもたらすことが示されています。(Hung et al. 2015, Guo et al. 2022, Guvvala et al. 2016, Yeh et al. 2007)

女性不妊
卵子は卵胞と呼ばれる細胞の集まりによって包まれ、育てられます。
この卵胞の死は卵胞閉鎖と呼ばれ、女性不妊と強く関連していることが示されています。(Yao et al. 2021)
そして、酸化ストレスが卵胞閉鎖に関与していることを示す証拠は増え続けています。(H. and M.H. 2012)
例えばマウスを使った実験では、農薬や藍藻毒などに起因する酸化ストレスにより、卵胞閉鎖が増加することが示されています。(Gupta et al. 2006, Wang et al. 2012, Dai et al. 2015, Wu et al. 2015)

記憶力の低下
ラットを使った動物実験では、高カロリー食や放射線などに起因する酸化ストレスにより、海馬をはじめとする脳細胞の死が増加し、記憶力が低下することが確認されています。(Maiti et al. 2008, Fukui et al. 2001, Treviño et al. 2015, MANDA et al. 2008)

発達障害
複数の研究を統合した分析で、ADHDと酸化ストレスの相関がみつかっています。(Joseph et al. 2013)
自閉症と酸化ストレスの相関も示されています。(James et al. 2004)

神経変性疾患
酸化ストレスはアルツハイマー病初期における顕著な特徴であり、その進行にも重要な役割を果たしています。(Wang et al. 2014)
酸化ストレスはALSの病因における主犯です。ALSの死後組織、実験モデルの双方において、活性酸素の増加が観察されています。(Carrı̀ et al. 2003)

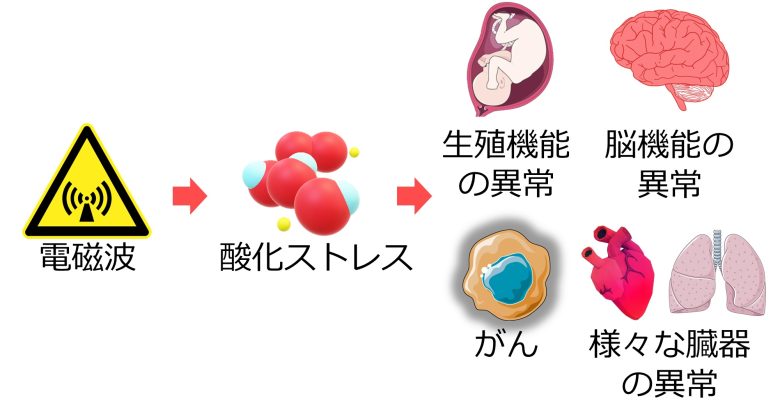
電磁波の健康影響は酸化ストレスで説明可能
生殖機能の異常、脳機能の異常、がん、様々な臓器の異常など、電磁波被曝によって極めて多岐に渡る疾患が増加することが示されています。
これらの多くは、電磁波の引き起こす酸化ストレスによって説明可能である、ということになります。

活性酸素は物質の分子構造を破壊する
活性酸素の分子構造
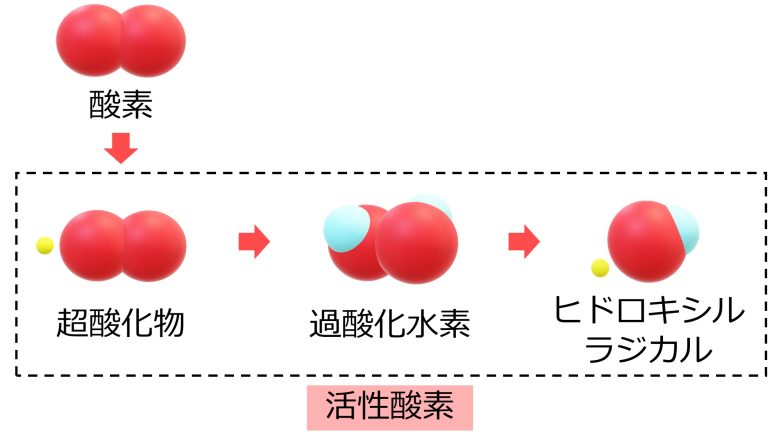
活性酸素の種類には、超酸化物、過酸化水素、ヒドロキシルラジカルなどがあります。
酸素が電子を一個うけとると超酸化物へと変化し、超酸化物は酵素などによって過酸化水素へと変化し、過酸化水素は周囲の金属イオンと反応し、ヒドロキシルラジカルへと変化します。

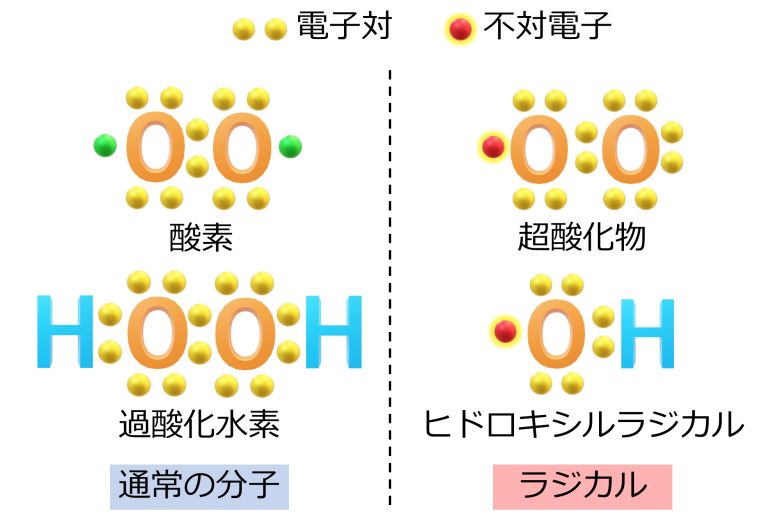
活性酸素のうち、超酸化物やヒドロキシルラジカルは、ラジカルと呼ばれる分子です。
通常の分子であれば電子がすべて2つずつ、ペアを組んで存在しているのですが、ラジカルにおいては電子がペアになってない不対電子が存在します。

この不対電子が存在するため、ラジカルは他の分子から電子を奪い取り、対象の分子構造を破壊するという危険な性質を持っています。
特にヒドロキシルラジカルは活性酸素の中でもっとも有害で、活性酸素によるDNAの酸化や切断の犯人です。
過酸化水素はラジカルではないですが、一定量が有害なヒドロキシルラジカルへと変化します。
したがって過酸化水素の増加はヒドロキシルラジカルの増加に直結するため、やはり細胞にとって危険な存在です。
活性酸素によるDNA切断
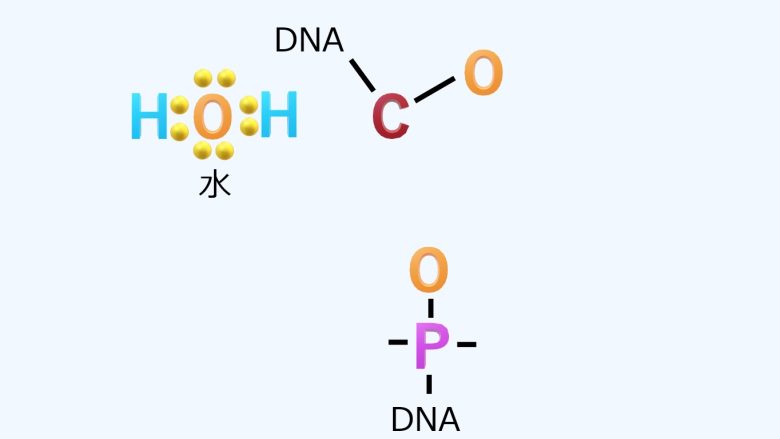
以下はヒドロキシルラジカルがDNAを切断する過程です。(Dumont and Monari 2015, Dedon et al. 1998)
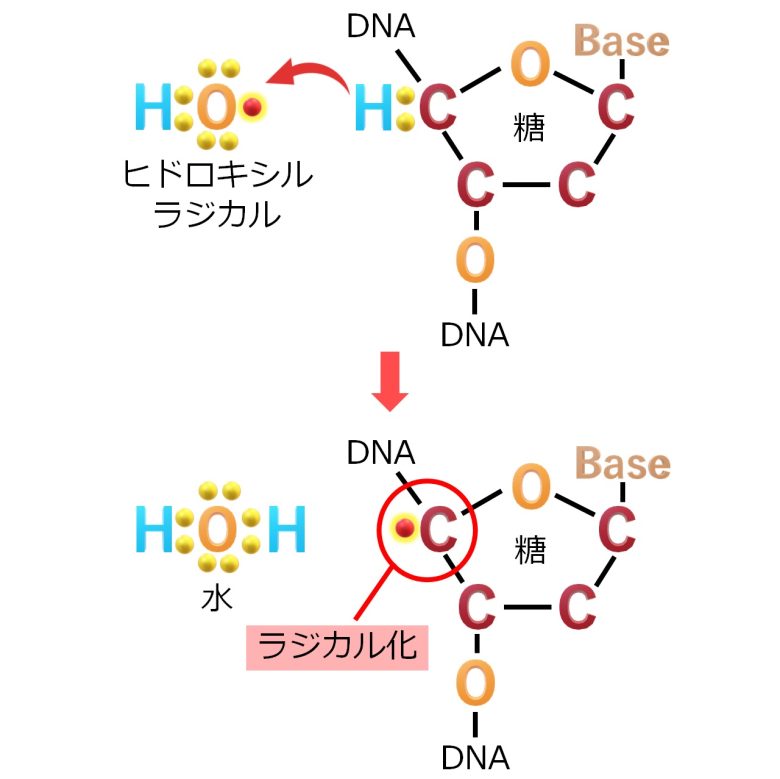
まずヒドロキシルラジカルはDNAの骨格である糖から、電子を水素原子ごと引き抜きます。
これにより自身は水分子となり安定しますが、今度は糖を構成する炭素原子がラジカル化してしまいます。
 ヒドロキシルラジカルによる炭素原子のラジカル化
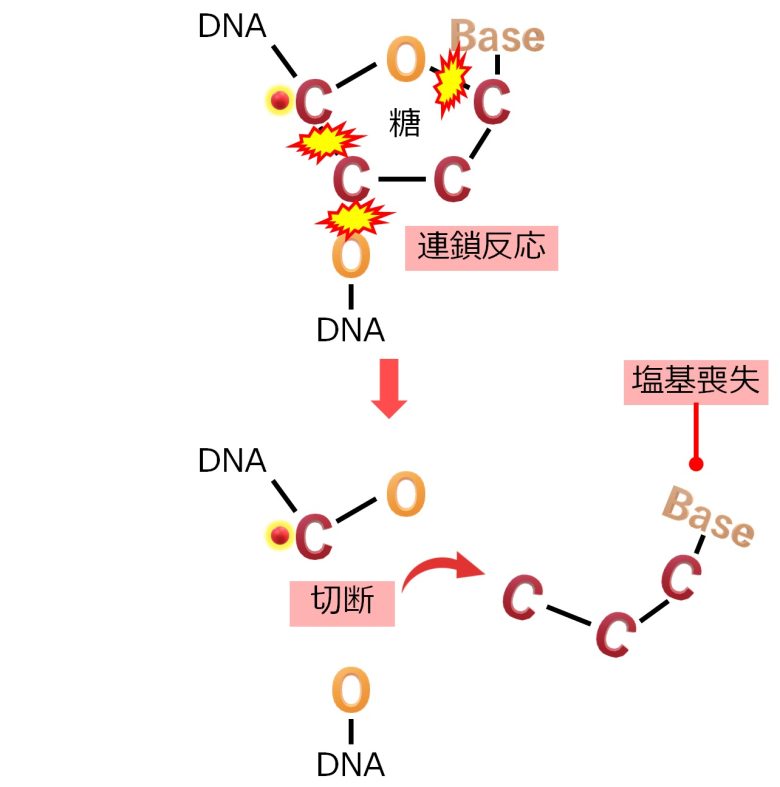
ヒドロキシルラジカルによる炭素原子のラジカル化続いて炭素ラジカルがさらに他の分子をラジカル化するという連鎖反応を起こし、ついにはDNAの切断に至ります。
この時、遺伝情報を担う塩基の喪失を伴うこともあります。
 炭素ラジカルによるDNAの切断
炭素ラジカルによるDNAの切断活性酸素による細胞損傷の経路
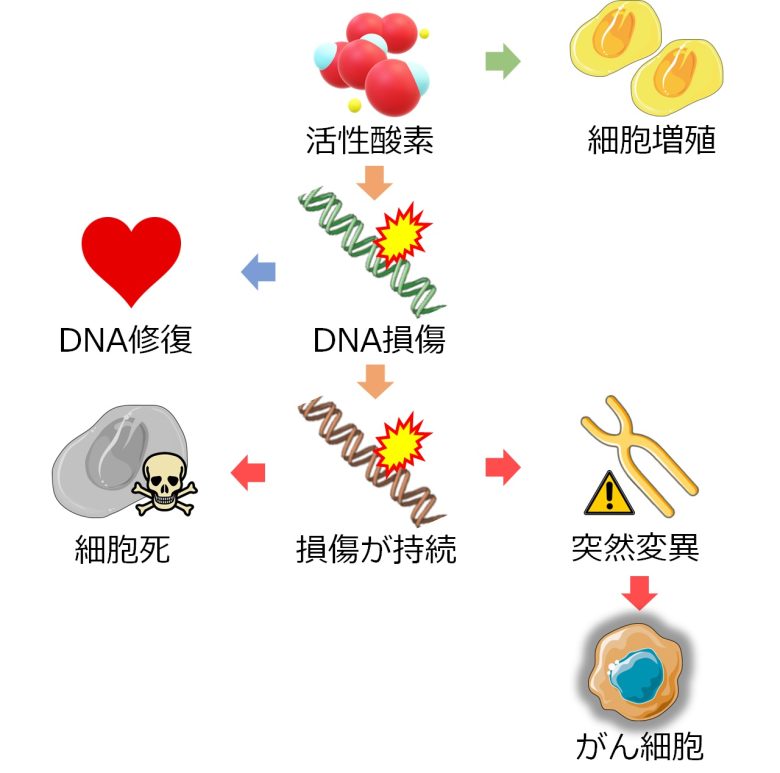
2011年のアメリカ・ギリシャの論文をもとに、活性酸素による細胞損傷の経路を紹介します。(Kryston et al. 2011)
- 内的・外的要因により活性酸素が発生する。
- 活性酸素によりDNAが損傷する。
- 損傷したDNAが修復を受ける。
- しかしDNA損傷が長続きすると、細胞死につながり、また突然変異が発生する。
- 突然変異により細胞のゲノム (全遺伝情報) は不安定になり、がん細胞と化す。
- 一方、活性酸素は逆に細胞増殖のシグナルとしても働く。
つまり電磁波を被曝すると体中の細胞で活性酸素が増加し、細胞死や突然変異がおきてしまうということです。
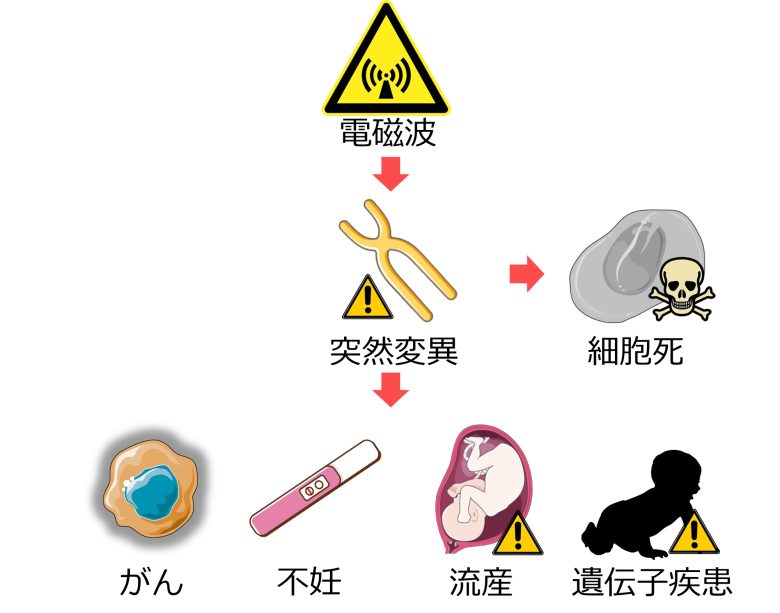
さらに突然変異は発がん、不妊、流産、遺伝子疾患などにつながり、健康に影響を与えます。
また、大規模な突然変異を起こした細胞を、細胞死へと誘導する機構が存在します。

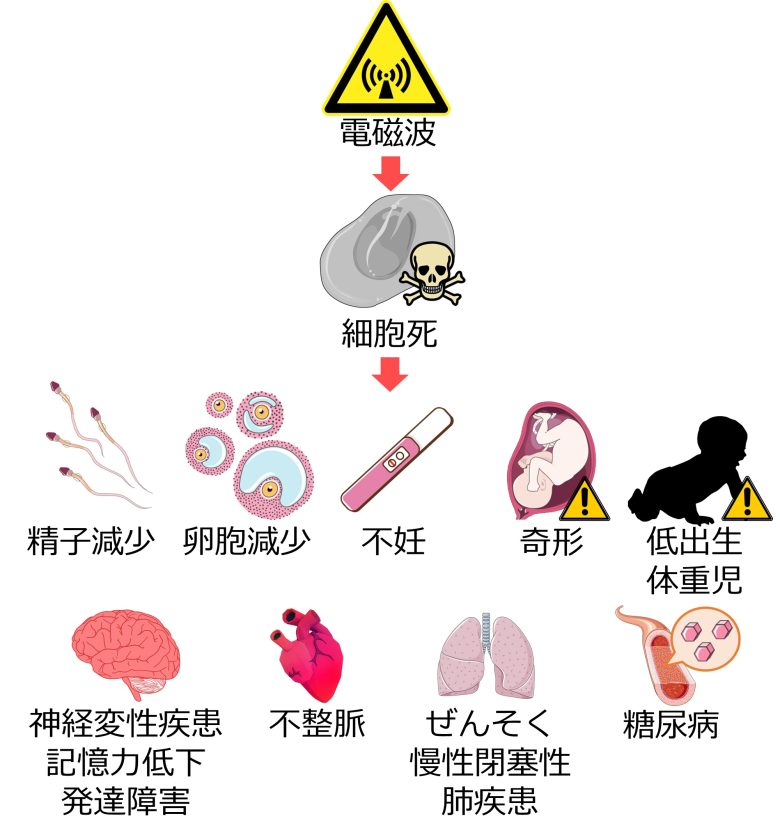
一方、細胞死は精子減少、卵胞減少、不妊、奇形、低出生体重児、神経変性疾患、記憶力低下、発達障害、不整脈、慢性閉塞性肺疾患、ぜんそく、糖尿病などにつながり、健康に影響を与えます。

上述した疾患はすべて、電磁波被曝で増加することが確認されています。
次のページから、活性酸素による細胞損傷の仕組み、またそこから数々の疾患へとつながる仕組みを説明します。
そして電磁波が、活性酸素による様々な細胞損傷を実際に引き起こすことを示した、多数の研究を紹介します。
DNA損傷